XANAX®
BEZPEČNOSŤ A ZNÁŠANLIVOSŤ
XANAX® SR je vo všeobecnosti dobre tolerovaný.1
XANAX® SR bol dobre znášaný v krátkodobých placebom kontrolovaných klinických skúšaniach.1
V prípade výskytu sa vedľajšie účinky lieku XANAX® vo všeobecnosti pozorujú na začiatku liečby a zvyčajne vymiznú v priebehu liečby.2
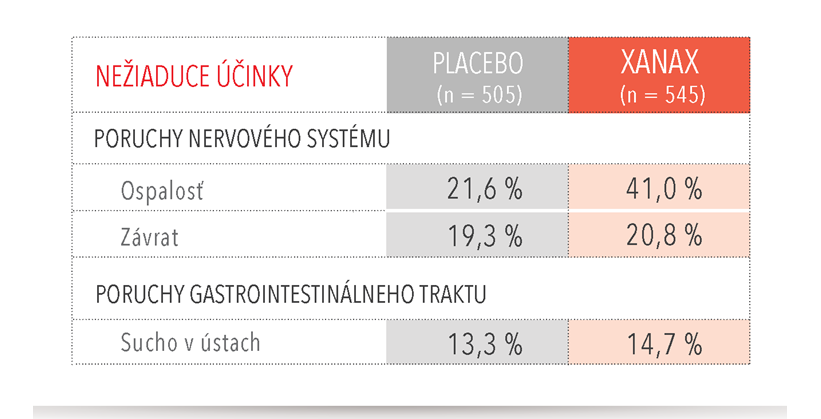
Nežiaduce účinky s ≥ 5 % incidenciou a vyššou v porovnaní s placebom.1

XANAX® je vo všeobecnosti dobre znášaný.3
V placebom kontrolovaných skúšaniach u pacientov s úzkostnými poruchami bol u lieku XANAX® preukázaný nízky výskyt nežiaducich udalostí.3
Nežiaduce účinky s ≥ 5 % incidenciou a vyššou v porovnaní s placebom.3
V porovnaní s diazepamom XANAX® v histórii klinického výskumu preukazuje nižší výskyt niekoľkých bežných vedľajších účinkov.4
XANAX® je dobre tolerovaný krátkodobo pôsobiaci benzodiazepín s výrazným znížením nasledujúcich nežiaducich účinkov v porovnaní s diazepamom (P < 0,005) v placebom kontrolovaných klinických skúšaniach:4
- Ospalosť
- Závrat
- Rozmazané videnie
- Depresia
- Zmätenosť
Informácie o bezpečnosti.2
- Benzodiazepíny vyvolávajú aditívny tlmivý účinok na centrálny nervový systém (CNS), vrátane respiračnej depresie, keď sa podávajú spolu s alkoholom alebo inými liekmi tlmiacimi CNS.
- Pri podávaní lieku XANAX® spolu s liekmi, ktoré interferujú s jeho metabolizmom, sa môžu vyskytnúť farmakokinetické interakcie. Niektoré látky inhibujúce pečeňové enzýmy (najmä cytochróm P450 3A4) môžu zvýšiť koncentráciu lieku XANAX® a zvýšiť jeho aktivitu.
- Nasledovné odporúčania sú založené na stupni interakcie a druhu dostupných údajov:
- Súbežné podávanie lieku XANAX® s ketokonazolom, itrakonazolom a ďaľšími azolovými antimykotikami sa neodporúča.
- Opatrnosť a zváženie redukcie dávky sa odporúča pri súbežnom podávaní lieku XANAX® s nefazodónom, fluvoxamínom a cimetidínom.
- Pri súbežnom podávaní lieku XANAX® s fluoxetínom, propoxyfénom, perorálnymi kontraceptívami, diltiazemom alebo makrolidovými antibiotikami, ako sú erytromycín, klaritromycín, telitromycín a troleandomycín, sa odporúča opatrnosť.
- Interakcie lieku XANAX® s inhibítormi HIV proteáz (napr. ritonavir) sú komplexné a závisia od trvania podávania. Nízke dávky ritonaviru spôsobili významné zmeny v klírense alprazolamu, predĺžený eliminačný polčas a zvýšenie jeho klinických účinkov. Avšak po dlhodobom podávaní ritonaviru sa mení jeho inhibičný účinok indukciou CYP3A. Takáto interakcia vyžaduje úpravu dávkovania alebo ukončenie liečby liekom XANAX®.
- Pri podávaní lieku XANAX® sa zaznamenali zvýšené koncentrácie digoxínu a to najmä u starších osôb (vo veku > 65 rokov). U pacientov, ktorí užívajú XANAX® a digoxín, je potrebné sledovať prejavy a príznaky spojené s toxicitou digoxínu.
Použitá literatúra:
- SPC Xanax® SR tablety s predĺženým uvoľňovaním, aktualizácia 12/2021.
- XANAX® [Core Data Sheet]. Pfizer Inc., November 20, 2018.
- SPC Xanax® tablety, aktualizácia 12/2021.
- Dawson GW, et al. Alprazolam: A review of its pharmacodynamic properties and efficacy in the treatment of anxiety and depression. Drugs. 1984;27(2):132-147.